
Πίνακας περιεχομένων:
- Συγγραφέας Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Τελευταία τροποποίηση 2025-01-22 16:57.
Ενα ιοντική ένωση είναι ένας γίγαντας δομή του ιόντων . ο ιόντα έχουν μια τακτική, επαναλαμβανόμενη διάταξη που ονομάζεται an ιοντικό πλέγμα . Αυτό είναι γιατί στερεά ιοντικές ενώσεις σχηματίζουν κρυστάλλους με κανονικά σχήματα.
Εξάλλου, γιατί υπάρχουν ιοντικές ενώσεις σε ένα κρυσταλλικό πλέγμα;
Οι ιδιότητες του ιοντικές ενώσεις ακολουθούν από τα κανονικά κρυσταλλικού πλέγματος διάταξη των σφιχτά συνδεδεμένων φορτισμένων σωματιδίων που τα αποτελούν. Ιονικές ενώσεις τείνουν να έχουν υψηλά σημεία τήξης και βρασμού, επειδή η έλξη μεταξύ ιόντων στο πλέγμα είναι πολύ δυνατό.
Ομοίως, τι είναι το ιοντικό πλέγμα; Ενα ιωνικός η ένωση αποτελείται από κατιόντα και ανιόντα α πλέγμα δομή. ο ιοντικό πλέγμα Η δομή συγκρατείται από τις ηλεκτροστατικές δυνάμεις έλξης μεταξύ των αντίθετα φορτισμένων ιόντων . Ένα μέταλλο ή ένα κράμα μετάλλου αποτελείται από κατιόντα μετάλλων και μια θάλασσα από μετατοπισμένα ηλεκτρόνια.
Εδώ, όλες οι ιοντικές ενώσεις είναι κρυσταλλικές;
Ατομο ιόντων μέσα σε ένα ιοντική ένωση συνήθως έχουν πολλαπλούς πλησιέστερους γείτονες, επομένως δεν θεωρούνται μέρος μορίων, αλλά μέρος ενός συνεχούς τρισδιάστατου δικτύου, συνήθως σε κρυστάλλινος δομή. Ιονικές ενώσεις έχουν συνήθως υψηλά σημεία τήξης και βρασμού και είναι σκληρά και εύθραυστα.
Ποια είναι τα 4 χαρακτηριστικά των ιοντικών ενώσεων;
Ακολουθεί μια σύντομη λίστα με τα κύρια ακίνητα:
- Σχηματίζουν κρυστάλλους.
- Έχουν υψηλότερες ενθαλπίες σύντηξης και εξάτμισης από τις μοριακές ενώσεις.
- Είναι σκληροί.
- Είναι εύθραυστα.
- Έχουν υψηλά σημεία τήξης και επίσης υψηλά σημεία βρασμού.
- Αγάγουν ηλεκτρισμό αλλά μόνο όταν είναι διαλυμένα στο νερό.
Συνιστάται:
Ποιες είναι οι δομικές μονάδες που αποτελούν τις ιοντικές ενώσεις και πώς ονομάζονται;

Για δυαδικές ιοντικές ενώσεις (ιοντικές ενώσεις που περιέχουν μόνο δύο τύπους στοιχείων), οι ενώσεις ονομάζονται γράφοντας πρώτα το όνομα του κατιόντος και μετά το όνομα του ανιόντος. Για παράδειγμα, το KCl, μια ιοντική ένωση που περιέχει ιόντα K+ και Cl-, ονομάζεται χλωριούχο κάλιο
Γιατί οι ιοντικές ενώσεις διαλύονται εύκολα στο νερό;

Για να διαλυθεί μια ιοντική ένωση, τα μόρια του νερού πρέπει να είναι σε θέση να σταθεροποιήσουν τα ιόντα που προκύπτουν από τη διάσπαση του ιοντικού δεσμού. Αυτό το κάνουν ενυδατώνοντας τα ιόντα. Το νερό είναι ένα πολικό μόριο. Όταν τοποθετείτε μια ιοντική ουσία στο νερό, τα μόρια του νερού προσελκύουν τα θετικά και αρνητικά ιόντα από τον κρύσταλλο
Όλες οι γραμμικές συναρτήσεις έχουν αντίστροφες;
Αντίστροφο μη σταθερών γραμμικών συναρτήσεων. Μια γραμμική συνάρτηση θα είναι αντιστρέψιμη όσο δεν είναι σταθερή, ή με άλλα λόγια έχει μη μηδενική κλίση. Μπορείτε να βρείτε το αντίστροφο είτε αλγεβρικά είτε γραφικά αντανακλώντας την αρχική γραμμή πάνω από τη διαγώνιο y = x
Πώς μοιάζουν όλες οι ενώσεις;

Εξήγηση: Οι ενώσεις όπως το CO2 αποτελούνται από άτομα ενωμένα για να δημιουργήσουν σταθερά μόρια. Όλες οι ενώσεις αποτελούνται πάντα από άτομα διαφορετικών τύπων για την παραγωγή μορίων. Τα στοιχεία όταν είναι μόρια αποτελούνται πάντα από άτομα του ίδιου τύπου
Πώς γράφετε τύπους για δυαδικές ιοντικές ενώσεις;
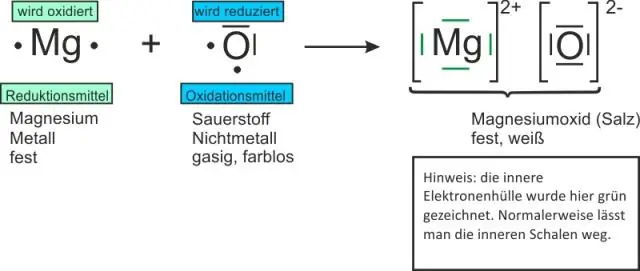
Οι τύποι για δυαδικές ενώσεις ξεκινούν με το μέταλλο που ακολουθείται από το αμέταλλο. Τα θετικά και τα αρνητικά φορτία πρέπει να αλληλοεξουδετερώνονται. Οι τύποι ιοντικών ενώσεων γράφονται χρησιμοποιώντας τη χαμηλότερη αναλογία ιόντων
