
- Συγγραφέας Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Τελευταία τροποποίηση 2025-01-22 16:57.
Χλώριο είναι ένα μη μέταλλο. ΕΝΑ χλώριο Το άτομο έχει 7 ηλεκτρόνια στο εξωτερικό του περίβλημα. με άλλα χλώριο άτομα. Ένα ζεύγος κοινών ηλεκτρονίων σχηματίζει ένα ενιαίο ομοιοπολικό δεσμός.
Ομοίως, το χλώριο είναι ιοντικό ή ομοιοπολικό;
Σε ομοιοπολική ομόλογα, όπως χλώριο αέριο (Cl2), και τα δύο άτομα μοιράζονται και συγκρατούνται σφιχτά το ένα πάνω στα ηλεκτρόνια του άλλου.
Στη συνέχεια, το ερώτημα είναι, είναι το cl2 ομοιοπολικός δεσμός; ΕΝΑ χλώριο Το άτομο έχει 7 ηλεκτρόνια στο κέλυφος σθένους του - χρειάζεται 8 για να το ολοκληρώσει. Δύο χλώριο Τα άτομα μπορούν να μοιράζονται 1 ηλεκτρόνιο το καθένα για να σχηματίσουν ένα ενιαίο ομοιοπολικό δεσμό . Γίνονται Cl2 μόριο.
Ομοίως, τι είναι ο ομοιοπολικός δεσμός με το χλώριο;
Ένα άλλο παράδειγμα του α ομοιοπολικό δεσμό είναι το Cl-Cl δεσμός σε ένα χλώριο μόριο. Δύο χλώριο άτομα έλκονται από το ίδιο ζεύγος ηλεκτρονίων. Καθε χλώριο άτομο συνεισφέρει ένα ηλεκτρόνιο στο συνδεδεμένο ζεύγος που μοιράζονται τα δύο άτομα. Τα υπόλοιπα έξι ηλεκτρόνια σθένους του καθενός χλώριο άτομο δεν εμπλέκονται σε συγκόλληση.
Τι είδους δεσμός σχηματίζεται μεταξύ του φωσφόρου και του χλωρίου;
Κάθε άτομο υδρογόνου χρειάζεται δύο ηλεκτρόνια για να επιτευχθεί ένα σταθερό εξωτερικό κέλυφος ηλεκτρονίων. Το ζεύγος ηλεκτρονίων έλκεται από το θετικό φορτίο και των δύο ατομικών πυρήνων, κρατώντας το μόριο ενωμένο. Φώσφορος μπορώ μορφή είτε PCl3 ή PCl5. Και στις δύο περιπτώσεις, το φώσφορο και χλώριο τα άτομα συνδέονται με ομοιοπολικό δεσμούς.
Συνιστάται:
Ποια είναι η ηλεκτρονική διαμόρφωση του χλωρίου σε διεγερμένη κατάσταση;

Ποια διάταξη ηλεκτρονίων αντιπροσωπεύει ένα άτομο χλωρίου σε διεγερμένη κατάσταση; (2) 2-8-6-1 αυτή είναι η διεγερμένη κατάσταση του χλωρίου, στον περιοδικό πίνακα η θεμελιώδης κατάσταση είναι 2-8-7. Η διαμόρφωση ηλεκτρονίων διεγερμένης κατάστασης δείχνει ένα ηλεκτρόνιο να αφήνει ένα ενεργειακό επίπεδο και να κινείται προς ένα υψηλότερο επίπεδο
Ποια είναι η διαφορά μεταξύ του ορισμού του Arrhenius και του ορισμού του brønsted Lowry για τα οξέα και τις βάσεις;

Η διαφορά μεταξύ των τριών θεωριών είναι ότι η θεωρία Arrhenius δηλώνει ότι τα οξέα περιέχουν πάντα Η+ και ότι οι βάσεις περιέχουν πάντα ΟΗ-. Ενώ το μοντέλο Bronsted-Lowry ισχυρίζεται ότι τα οξέα είναι δότες πρωτονίων και δέκτες pron, επομένως οι βάσεις δεν χρειάζεται να περιέχουν OH- έτσι τα οξέα δίνουν ένα πρωτόνιο στο νερό που σχηματίζει H3O+
Ποια είναι η τυπική κατάσταση του χλωρίου;

Το χλώριο είναι ένα πρασινωπό κίτρινο αέριο σε θερμοκρασία δωματίου και ατμοσφαιρική πίεση. Είναι δυόμιση φορές βαρύτερο από τον αέρα. Γίνεται υγρό στους −34 °C (−29 °F)
Ποια είναι η σύνδεση των στατιστικών στην πιθανότητα;
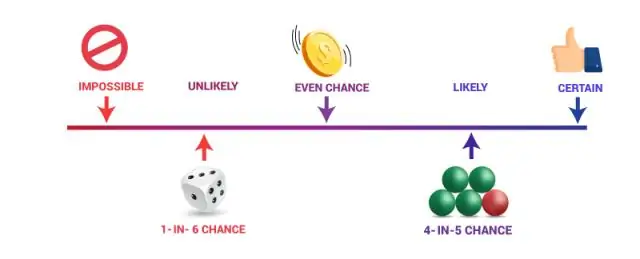
Οι πιθανότητες και η στατιστική είναι σχετικοί τομείς των μαθηματικών που ασχολούνται με την ανάλυση της σχετικής συχνότητας των γεγονότων. Η πιθανότητα ασχολείται με την πρόβλεψη της πιθανότητας μελλοντικών γεγονότων, ενώ η στατιστική περιλαμβάνει την ανάλυση της συχνότητας των προηγούμενων γεγονότων
Ποια είναι η λειτουργική σύνδεση μεταξύ των πυρηνικών πόρων του πυρήνα και της πυρηνικής μεμβράνης;

Ποια είναι η λειτουργική σύνδεση μεταξύ του πυρήνα, των πυρηνικών πόρων και της πυρηνικής μεμβράνης; Α. Ο πυρήνας περιέχει αγγελιοφόρο RNA (mRNA), το οποίο διασχίζει το πυρηνικό περίβλημα μέσω των πυρηνικών πόρων
