
- Συγγραφέας Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Τελευταία τροποποίηση 2025-01-22 16:57.
Ορισμός. Δυνάμεις Van der Waals περιλαμβάνει έλξη και απώθηση μεταξύ ατόμων, μορίων και επιφανειών, καθώς και άλλα διαμοριακά δυνάμεις . Διαφέρουν από τον ομοιοπολικό και τον ιοντικό δεσμό στο ότι είναι που προκαλούνται από συσχετίσεις στις κυμαινόμενες πόλώσεις των κοντινών σωματιδίων (συνέπεια της κβαντικής δυναμικής).
Λοιπόν, πού βρίσκονται οι δυνάμεις του van der Waals;
Καλά, Δυνάμεις Van der Waals είναι παρόν σε όλες τις αλληλεπιδράσεις μεταξύ ομοιοπολικών μορίων και μη μετάλλων. Για υπενθύμιση, πιθανότατα έχετε ακούσει για το πώς τα μόρια του νερού επηρεάζονται από τα σχετικά ισχυρά Van Der Waals , δεσμός υδρογόνου.
Ομοίως, ποιες είναι οι δυνάμεις van der Waals στη χημεία; Δυνάμεις Van der Waals ' είναι ένας γενικός όρος που χρησιμοποιείται για να ορίσει την έλξη των διαμοριακών δυνάμεις μεταξύ των μορίων. Υπάρχουν δύο είδη Δυνάμεις Van der Waals : ασθενής διασπορά Λονδίνου Δυνάμεις και ισχυρότερο δίπολο-δίπολο δυνάμεις.
Έχοντας αυτό υπόψη, πώς υπολογίζονται οι δυνάμεις του van der Waals;
Εξίσωση Van der Waals Το V στο τύπος αναφέρεται στον όγκο του αερίου, σε moles n. Το διαμοριακό δυνάμεις της έλξης ενσωματώνονται στο εξίσωση με το n 2 a V 2 frac{n^2a}{V^2} V2n2a; όρος όπου a a α είναι μια συγκεκριμένη τιμή ενός συγκεκριμένου αερίου.
Ποιοι είναι οι τρεις τύποι δυνάμεων van der Waals;
Οι τρεις τύποι δυνάμεων van der Waals περιλαμβάνουν: 1) διασπορά (αδύναμη), 2) δίπολο - δίπολο (μεσαίο) και 3) υδρογόνο (ισχυρό). Ιόν- δίπολο δεσμοί (ιοντικά είδη προς ομοιοπολικά μόρια) σχηματίζονται μεταξύ ιόντων και πολικών μορίων.
Συνιστάται:
Πώς ονομάζεται το άλας που σχηματίζεται από την εξουδετέρωση του υδροχλωρικού οξέος και του υδροξειδίου του νατρίου;
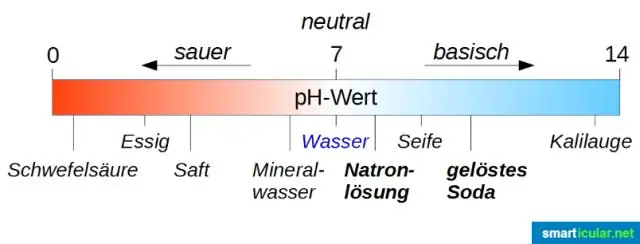
Εξήγηση: Η αντίδραση μεταξύ υδροξειδίου του νατρίου (NaOH) και υδροχλωρικού οξέος (HCl) είναι μια αντίδραση εξουδετέρωσης που έχει ως αποτέλεσμα το σχηματισμό άλατος, χλωριούχου νατρίου (NaCl) και νερού (H2O). Είναι μια εξώθερμη αντίδραση
Ποιες δυνάμεις δρουν σε αντικείμενα που δεν κινούνται;

Η τριβή είναι μια δύναμη που αντιτίθεται στην κίνηση των αντικειμένων που αγγίζουν καθώς περνούν το ένα δίπλα στο άλλο. Η στατική τριβή είναι η δύναμη τριβής που δρα σε αντικείμενα που δεν κινούνται. Η στατική τριβή δρα πάντα προς την αντίθετη κατεύθυνση από αυτήν της ασκούμενης δύναμης
Ποιος είναι ο σωστός τύπος του άλατος που σχηματίζεται στην αντίδραση εξουδετέρωσης του υδροχλωρικού οξέος με το υδροξείδιο του βαρίου;

Ερώτηση: Ποιος είναι ο σωστός τύπος του άλατος που σχηματίζεται στην αντίδραση εξουδετέρωσης του υδροχλωρικού οξέος με το υδροξείδιο του βαρίου; BaCl BaCl2 BaClH BaH2 BaO
Ποιες είναι οι μόνες τέσσερις δυνάμεις που μπορούν να επηρεάσουν την ύλη;

Οι τέσσερις βασικές δυνάμεις είναι η βαρυτική δύναμη, η ηλεκτρομαγνητική δύναμη, η ασθενής πυρηνική δύναμη και η ισχυρή πυρηνική δύναμη
Ποια είναι η έννοια του van der Waals;

Οι δυνάμεις Van der Waals είναι ένας γενικός όρος που χρησιμοποιείται για να ορίσει την έλξη των διαμοριακών δυνάμεων μεταξύ των μορίων. Υπάρχουν δύο είδη δυνάμεων Van der Waals: αδύναμες δυνάμεις διασποράς του Λονδίνου και ισχυρότερες δυνάμεις διπόλου-διπόλου
