
- Συγγραφέας Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Τελευταία τροποποίηση 2025-06-01 05:04.
Θεωρώντας τα ίδια στοιχεία Α και Β για να σχηματίσετε το α μη - ιδανική λύση , αυτό θα δείχνουν αρνητικά απόκλιση από το νόμο του Raoult μόνο όταν: Η αλληλεπίδραση διαλυμένης ουσίας-διαλύτη είναι ισχυρότερη από την αλληλεπίδραση διαλυμένης ουσίας και διαλύτη-διαλύτη που είναι , A - B > A - A ή B - B.
Με αυτόν τον τρόπο, τι προκαλεί θετική απόκλιση από το Νόμο του Raoult;
Εάν η διαλυμένη ουσία και ο διαλύτης δεν είναι τόσο στενά συνδεδεμένα μεταξύ τους όσο με τον εαυτό τους, τότε το διάλυμα θα δείξει θετική απόκλιση από το νόμο του Raoult επειδή τα μόρια του διαλύτη θα είναι πιο εύκολο να διαφύγουν από το διάλυμα στην αέρια φάση.
Στη συνέχεια, το ερώτημα είναι ποια είναι η ιδανική και η μη ιδανική λύση ποιος τύπος μη ιδανικής απόκλισης εμφανίζεται από το μείγμα χλωροφορμίου και ακετόνης; Απάντηση: Μίγμα χλωροφορμίου και ακετόνης show -ve απόκλιση από τον νόμο του Raoult. Ιδανικές λύσεις είναι οι λύσεις που υπακούουν στο νόμο του Raoult σε κάθε θερμοκρασία και συγκέντρωση ενώ μη ιδανικές λύσεις αποκλίνουν από το νόμο του Raoult σε διαφορετικές συγκεντρώσεις και θερμοκρασίες.
Εδώ, ποια είναι η ιδανική λύση και ποια η μη ιδανική λύση;
ΕΝΑ μη - ιδανική λύση είναι ένα λύση που δεν τηρεί τους κανόνες μιας ιδανική λύση όπου οι αλληλεπιδράσεις μεταξύ των μορίων είναι πανομοιότυπες (ή πολύ κοντινές) με τις αλληλεπιδράσεις μεταξύ μορίων διαφορετικών συστατικών. Υποθέτουμε ιδανικός ιδιότητες για αραίωση λύσεις.
Τι σημαίνει θετική και αρνητική απόκλιση από το νόμο του Raoult;
Ο νόμος του Ραούλ δηλώνει ότι σε μια δεδομένη θερμοκρασία, η τάση ατμών ενός διαλύματος που περιέχει μη πτητική διαλυμένη ουσία είναι ευθέως ανάλογη του μοριακού κλάσματος του διαλύτη. Οι μη ιδανικές λύσεις δείχνουν θετικός & αρνητικές αποκλίσεις από ιδανική συμπεριφορά.
Συνιστάται:
Πώς λύνετε τον νόμο του ιδανικού αερίου;

Τύπος του νόμου του ιδανικού αερίου Ερωτήσεις για τον τύπο του νόμου του ιδανικού αερίου: Απάντηση: Ο όγκος είναι V = 890,0 mL και η θερμοκρασία είναι T = 21°C και η πίεση είναι P = 750 mmHg. PV = nRT. Απάντηση: Ο αριθμός των moles είναι n = 3,00moles, η θερμοκρασία είναι T = 24°C και η πίεση είναι P = 762,4 mmHg. PV = nRT
Πώς ανακάλυψε ο Μέντελ τον νόμο του διαχωρισμού;

Οι αρχές που διέπουν την κληρονομικότητα ανακαλύφθηκαν από έναν μοναχό ονόματι Γκρέγκορ Μέντελ τη δεκαετία του 1860. Μία από αυτές τις αρχές, που τώρα ονομάζεται νόμος του διαχωρισμού του Mendel, δηλώνει ότι τα ζεύγη αλληλόμορφων διαχωρίζονται ή διαχωρίζονται κατά τη διάρκεια του σχηματισμού γαμετών και ενώνονται τυχαία κατά τη γονιμοποίηση
Μπορούμε να εφαρμόσουμε τον τρίτο νόμο του Νεύτωνα στη βαρυτική δύναμη;
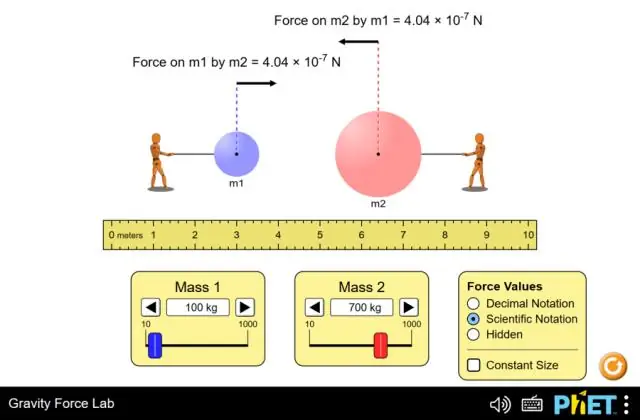
Ναι, ο τρίτος νόμος του Νεύτωνα ισχύει για τη βαρυτική δύναμη. Ως εκ τούτου, Αυτό σημαίνει ότι όταν η γη μας ασκεί μια δύναμη έλξης σε ένα αντικείμενο, τότε το αντικείμενο ασκεί επίσης ίση δύναμη στη γη, προς την αντίθετη κατεύθυνση. Ως εκ τούτου, μπορούμε να πούμε ότι μπορείτε να εφαρμόσετε τον τρίτο νόμο του Νεύτωνα στη βαρυτική δύναμη
Γιατί ο νόμος του Lenz είναι συνεπής με τον νόμο της διατήρησης της ενέργειας;

Ο νόμος του Lenz είναι συνεπής με την Αρχή της Διατήρησης της Ενέργειας επειδή όταν ένας μαγνήτης με πηνίο που βλέπει προς τον Ν πόλο ωθείται προς το πηνίο (ή τραβιέται μακριά από), υπάρχει αύξηση (ή μείωση) στη σύνδεση μαγνητικής ροής, με αποτέλεσμα μια επαγόμενη ρεύμα που ρέει στο κελί, σύμφωνα με το νόμο του Faraday
Πώς αποδεικνύετε το νόμο του Raoult;

Να αναφέρετε και να αποδείξετε το νόμο του Raoult για τη μη πτητική διαλυμένη ουσία σε πτητικό διαλύτη. Δώστε επίσης δύο περιορισμούς του νόμου του Raoult. Η τάση ατμών ενός διαλύματος μιας μη πτητικής διαλυμένης ουσίας είναι ίση με την τάση ατμών του καθαρού διαλύτη στη θερμοκρασία αυτή πολλαπλασιαζόμενη με το μοριακό του κλάσμα
