
Πίνακας περιεχομένων:
- Συγγραφέας Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Τελευταία τροποποίηση 2025-01-22 16:57.
Γράφοντας το διαμόρφωση ηλεκτρονίων για οξυγόνο τα πρώτα δύο ηλεκτρόνια θα πάει στο τροχιακό 1s. Αφού το 1 χωράει μόνο δύο ηλεκτρόνια τα επόμενα 2 ηλεκτρόνια για το O πηγαίνετε στο τροχιακό 2s. Τα υπόλοιπα τέσσερα ηλεκτρόνια θα πάει στο τροχιακό 2p. Επομένως το Ο διαμόρφωση ηλεκτρονίων θα είναι 1 δευτ22s22π4.
Εξάλλου, πώς βρίσκετε τη διαμόρφωση ηλεκτρονίων;
Βήματα
- Βρείτε τον ατομικό αριθμό του ατόμου σας.
- Προσδιορίστε το φορτίο του ατόμου.
- Απομνημονεύστε τη βασική λίστα των τροχιακών.
- Κατανόηση του συμβολισμού της διαμόρφωσης ηλεκτρονίων.
- Απομνημονεύστε τη σειρά των τροχιακών.
- Συμπληρώστε τα τροχιακά σύμφωνα με τον αριθμό των ηλεκτρονίων στο άτομό σας.
- Χρησιμοποιήστε τον περιοδικό πίνακα ως οπτική συντόμευση.
Επίσης, ποια είναι η διαμόρφωση ηλεκτρονίων του ιόντος οξειδίου o2 −); Σε οξείδιο , οξυγόνο έχει δύο επιπλέον ηλεκτρόνια να έχουμε οκταδική σταθερή κατάσταση. Ετσι, ηλεκτρονική διαμόρφωση του ιόν οξειδίου είναι: 1s2, 2s2 2p6.
Ομοίως, μπορεί κανείς να ρωτήσει, ποια είναι η διαμόρφωση ηλεκτρονίων για το κουίζ οξυγόνου;
Δεδομένου ότι το διαμόρφωση ηλεκτρονίων για οξυγόνο είναι 1s2 2s2 2p4 απαντήστε στις παρακάτω ερωτήσεις: α.
Τι είναι ο κανόνας των Hund;
Κανόνας του Hund . Ο κανόνας του Hund : κάθε τροχιακό σε ένα υποκέλυφος καταλαμβάνεται μεμονωμένα με ένα ηλεκτρόνιο πριν από οποιοδήποτε τροχιακό καταληφθεί διπλά, και όλα τα ηλεκτρόνια σε μεμονωμένα κατειλημμένα τροχιακά έχουν το ίδιο σπιν.
Συνιστάται:
Ποια είναι η διαμόρφωση ηλεκτρονίων σθένους πυρήνα για το άζωτο;
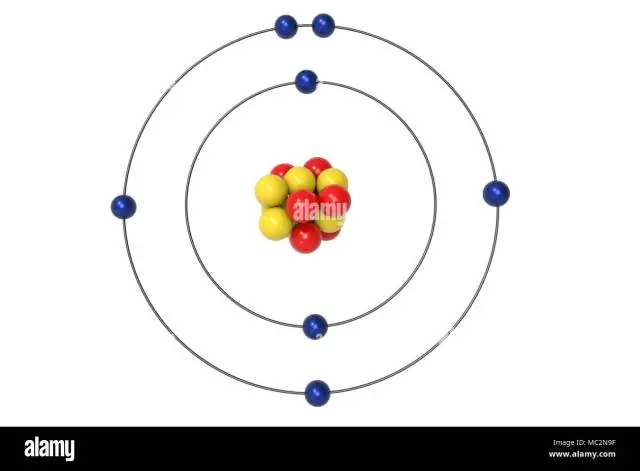
Τα υπόλοιπα τρία ηλεκτρόνια θα πάνε στο τροχιακό 2p. Επομένως, η διαμόρφωση ηλεκτρονίων Ν θα είναι 1s22s22p3. Ο συμβολισμός διαμόρφωσης για το άζωτο (N) παρέχει έναν εύκολο τρόπο για τους επιστήμονες να γράψουν και να επικοινωνήσουν πώς τα ηλεκτρόνια είναι διατεταγμένα γύρω από τον πυρήνα του ατόμου του αζώτου
Ποια είναι η πλήρης διαμόρφωση ηλεκτρονίων θεμελιώδους κατάστασης για το άτομο του γαλλίου;

Η διαμόρφωση ηλεκτρονίων θεμελιώδους κατάστασης του αέριου ουδέτερου γαλλίου θεμελιώδους κατάστασης είναι [Ar]. 3d10. 4s2. 4p1 και το σύμβολο του όρου είναι 2P1/2
Ποια είναι η διαμόρφωση ηλεκτρονίων για ένα άτομο ασβεστίου;

[Ar] 4s²
Πώς γράφετε τη διαμόρφωση ηλεκτρονίων για το MN;

Το μαγγάνιο, από την άλλη πλευρά, έχει μια διάταξη ηλεκτρονίων 1s22s22p63s23p64s23d5 και μια διαμόρφωση ευγενών αερίων [Ar]4s23d5, με αποτέλεσμα ένα μη ζευγαρωμένο ηλεκτρόνιο σε κάθε 3d υποτροχιακό
Πώς βρίσκετε τη διαμόρφωση ηλεκτρονίων για το ασήμι;

Η διαμόρφωση ηλεκτρονίων θεμελιώδους κατάστασης του αέριου ουδέτερου αργύρου θεμελιώδους κατάστασης είναι [Kr]. 4d10. 5s1 και το σύμβολο του όρου είναι 2S1/2
