
- Συγγραφέας Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Τελευταία τροποποίηση 2025-01-22 16:57.
Ενα στοιχειώδες βήμα (ή στοιχειώδης αντίδραση ) είναι ένα βήμα σε μια σειρά απλών αντιδράσεις που δείχνουν την πρόοδο του α αντίδραση σε μοριακό επίπεδο. ΕΝΑ μηχανισμός αντίδρασης είναι η ακολουθία του στοιχειώδη βήματα που μαζί αποτελούν μια ολόκληρη χημική ουσία αντίδραση.
Εκτός από αυτό, ποιο είναι ένα στοιχειώδες βήμα σε μια χημική αντίδραση;
Ενα στοιχειώδης διαδικασία ονομάζεται επίσης an στοιχειώδες βήμα ή στοιχειώδης αντίδραση . Εκφράζει πώς πραγματικά τα μόρια ή τα ιόντα αντιδρώ ο ένας με τον άλλο. ο εξίσωση σε μια στοιχειώδες βήμα αντιπροσωπεύει το αντίδραση σε μοριακό επίπεδο, όχι συνολικά αντίδραση.
Ομοίως, ποιος είναι ο μηχανισμός μιας αντίδρασης; Στη χημεία, α μηχανισμός αντίδρασης είναι η βήμα προς βήμα ακολουθία του δημοτικού αντιδράσεις με την οποία επέρχεται συνολική χημική αλλαγή. Μια χημική ουσία μηχανισμός είναι μια θεωρητική εικασία που προσπαθεί να περιγράψει λεπτομερώς τι συμβαίνει σε κάθε στάδιο μιας συνολικής χημικής ουσίας αντίδραση.
Σχετικά με αυτό, πόσα στοιχειώδη βήματα υπάρχουν στον μηχανισμό αντίδρασης;
2 δημοτικό
Τι είναι η αντίδραση πρώτης τάξης;
ΕΝΑ πρώτα - παραγγελία αντίδρασης είναι ένα αντίδραση που προχωρά με ρυθμό που εξαρτάται γραμμικά από μία μόνο συγκέντρωση αντιδρώντος.
Συνιστάται:
Τι επίδραση έχει ένας καταλύτης στον μηχανισμό μιας αντίδρασης;

Ένας καταλύτης επιταχύνει μια χημική αντίδραση, χωρίς να καταναλωθεί από την αντίδραση. Αυξάνει τον ρυθμό αντίδρασης μειώνοντας την ενέργεια ενεργοποίησης για μια αντίδραση
Πώς βρίσκετε το πιο αργό βήμα σε έναν μηχανισμό;

Τα ενδιάμεσα της αντίδρασης σχηματίζονται σε ένα στάδιο και στη συνέχεια καταναλώνονται σε ένα μεταγενέστερο στάδιο του μηχανισμού αντίδρασης. Το πιο αργό βήμα στον μηχανισμό ονομάζεται βήμα καθορισμού ρυθμού ή περιορισμού ρυθμού. Ο συνολικός ρυθμός αντίδρασης καθορίζεται από τους ρυθμούς των σταδίων μέχρι (και συμπεριλαμβανομένου) του σταδίου καθορισμού της ταχύτητας
Πώς κάνετε τη διαμόρφωση ηλεκτρονίων βήμα προς βήμα;

Βήματα Βρείτε τον ατομικό αριθμό του ατόμου σας. Προσδιορίστε το φορτίο του ατόμου. Απομνημονεύστε τη βασική λίστα των τροχιακών. Κατανόηση του συμβολισμού της διαμόρφωσης ηλεκτρονίων. Απομνημονεύστε τη σειρά των τροχιακών. Συμπληρώστε τα τροχιακά σύμφωνα με τον αριθμό των ηλεκτρονίων στο άτομό σας. Χρησιμοποιήστε τον περιοδικό πίνακα ως οπτική συντόμευση
Πώς γράφετε μια εξίσωση βήμα προς βήμα;
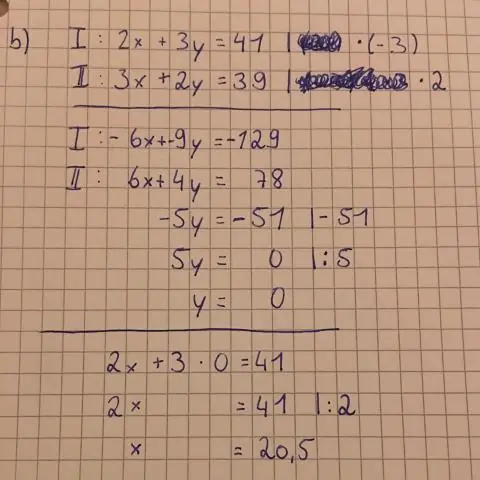
Ακολουθούν μερικά βήματα που πρέπει να ακολουθήσετε: Συνδέστε το x = 0 στην εξίσωση και λύστε το y. Σχεδιάστε το σημείο (0,y) στον άξονα y. Συνδέστε το y = 0 στην εξίσωση και λύστε το x. Σχεδιάστε το σημείο (x,0) στον άξονα x. Σχεδιάστε μια ευθεία γραμμή μεταξύ των δύο σημείων
Ποιο βήμα καθορίζει τον ρυθμό αντίδρασης;

Το βήμα προσδιορισμού του ρυθμού είναι το πιο αργό βήμα μιας χημικής αντίδρασης που καθορίζει την ταχύτητα (ταχύτητα) με την οποία προχωρά η συνολική αντίδραση. Το βήμα καθορισμού του ρυθμού μπορεί να συγκριθεί με το λαιμό μιας χοάνης
