
- Συγγραφέας Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Τελευταία τροποποίηση 2025-01-22 16:57.
| Θερμοκρασία (K) | ντοΠ (J/mol*K) | H° - H°298.15 (kJ/mol) |
|---|---|---|
| 298. | 59.52 | -0.00 |
| 300. | 59.67 | 0.12 |
| 400. | 64.94 | 6.34 |
| 500. | 75.16 | 13.29 |
Αντίστοιχα, ποια είναι η ειδική θερμοχωρητικότητα του HCl και του NaOH;
Ειδική Θερμότητα του HCl & NaOH Διάλυμα=4,017 J/g°C.
Επίσης, ποια είναι η ενθαλπία του nacl; Έτσι, όταν 1 mole από χλωριούχο νάτριο οι κρύσταλλοι διαλύονται σε περίσσεια νερού, η ενθαλπία Η μεταβολή του διαλύματος βρέθηκε να είναι +3,9 kJ mol-1. Η αλλαγή είναι ελαφρώς ενδόθερμη και έτσι η θερμοκρασία του διαλύματος θα είναι ελαφρώς χαμηλότερη από αυτή του αρχικού νερού.
Ομοίως, ποιες είναι οι χρήσεις του υδροξειδίου του νατρίου;
- Είναι βασικό συστατικό στα καθαριστικά αποχέτευσης και φούρνου.
- Χρησιμοποιείται στη χημική κατασκευή, τη διύλιση λαδιού, την υδραυλική θραύση, την επεξεργασία νερού και την επεξεργασία μετάλλων.
- Χρησιμοποιείται στην κατασκευή υφασμάτων, πλαστικών περιβλημάτων, χαρτιού και σαπουνιού.
Πώς υπολογίζετε την ειδική θερμοχωρητικότητα;
Οι μονάδες του ειδική θερμοχωρητικότητα είναι J/(kg °C) ή ισοδύναμα J/(kg K). ο θερμοχωρητικότητα και το ειδική θερμότητα σχετίζονται με C=cm ή c=C/m. Η μάζα m, ειδική θερμότητα γ, μεταβολή της θερμοκρασίας ΔT, και θερμότητα προστίθενται (ή αφαιρούνται) Q σχετίζονται με το εξίσωση : Q=mcΔT.
Συνιστάται:
Ποια είναι τα προϊόντα της μοριακής εξίσωσης για την αντίδραση πλήρους εξουδετέρωσης του υδατικού υδροξειδίου του βαρίου και του νιτρικού οξέος;

Ba(OH)2 + 2HNO3 → Ba(NO3)2 + 2H2O. Το υδροξείδιο του βαρίου αντιδρά με το νιτρικό οξύ για να παράγει νιτρικό βάριο και νερό
Πώς ονομάζεται το άλας που σχηματίζεται από την εξουδετέρωση του υδροχλωρικού οξέος και του υδροξειδίου του νατρίου;
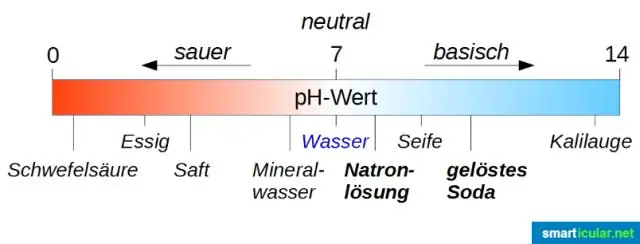
Εξήγηση: Η αντίδραση μεταξύ υδροξειδίου του νατρίου (NaOH) και υδροχλωρικού οξέος (HCl) είναι μια αντίδραση εξουδετέρωσης που έχει ως αποτέλεσμα το σχηματισμό άλατος, χλωριούχου νατρίου (NaCl) και νερού (H2O). Είναι μια εξώθερμη αντίδραση
Ποια είναι η ειδική θερμοχωρητικότητα του οκτανίου;

Ονομασίες οκτανίων Θερμοχωρητικότητα (C) 255,68 J K&μείον;1 mol&μείον;1 Std μοριακή εντροπία (So298) 361,20 J K&μείον;1 mol&μείον;1 Std ενθαλπία σχηματισμού (&Δέλτα;fH?298) &μείον;252,1 mol; 1 Std ενθαλπία καύσης (ΔcH?298) &μείον;5,53–&μείον;5,33 MJ mol&μείον;1
Ποια είναι η χρήση του υδροξειδίου του αμμωνίου;

καθάρισμα Ρωτήθηκε επίσης, ποιος είναι ο ρόλος του υδροξειδίου του αμμωνίου; Υδροξείδιο του αμμωνίου είναι αλκαλικό, που σημαίνει ότι έχει υψηλό pH, επομένως μπορεί να χρησιμοποιηθεί για την εξουδετέρωση των οξέων. Υδροξείδιο του αμμωνίου βρίσκεται φυσικά στον αέρα, το νερό και το έδαφος, ακόμη και μέσα στους ανθρώπους και τα φυτά.
Πόσα γραμμάρια υδροξειδίου του νατρίου υπάρχουν σε ένα διάλυμα 2 m;

Ο όρος 2Μ NaOH είναι η συντομογραφία του διαλύματος υδροξειδίου του μοριακού νατρίου 2. Αυτή η έκφραση σημαίνει ότι 2 moles (ή 2 x 40 g = 80 g) NaOH διαλύονται σε αρκετό νερό για να παραχθεί ένα λίτρο διαλύματος
