
- Συγγραφέας Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Τελευταία τροποποίηση 2025-01-22 16:57.
Environmental Science For Ανδρείκελα
Όταν δύο άτομα ενώνονται μεταξύ τους σε α ομοιοπολικό δεσμό , σχηματίζουν ένα μόριο που μοιράζεται ηλεκτρόνια. Σε αντίθεση με το ιοντικό δεσμός , κανένα από τα άτομα στο α ομοιοπολικό δεσμό χάνει ή κερδίζει ένα ηλεκτρόνιο. Αντίθετα, και τα δύο άτομα χρησιμοποιούν ένα ζεύγος κοινών ηλεκτρονίων.
Εξάλλου, τι είναι απλοί όροι ομοιοπολικός δεσμός;
Ομοιοπολικούς δεσμούς είναι χημικά δεσμούς μεταξύ δύο ατόμων μη μετάλλου. Ένα παράδειγμα είναι το νερό, όπου υδρογόνο (Η) και οξυγόνο (Ο) δεσμός μαζί για να φτιάξουμε (H2Ο). Ένα πλήρες εξωτερικό περίβλημα έχει συνήθως οκτώ ηλεκτρόνια, ή δύο στην περίπτωση του υδρογόνου ή του ηλίου. Ομοιοπολικούς δεσμούς σχηματίζονται από άτομα που μοιράζονται ηλεκτρόνια σθένους.
Στη συνέχεια, το ερώτημα είναι, τι είναι ένας ιοντικός δεσμός για τα ανδρείκελα; Environmental Science For Ανδρείκελα Για να σχηματίσουν μόρια, τα άτομα πρέπει να ανταλλάσσουν ή να μοιράζονται ηλεκτρόνια από το εξωτερικό τους κέλυφος ηλεκτρονίων για να δημιουργήσουν ατομικό δεσμούς . Ενα ιοντικός δεσμός συμβαίνει όταν ένα άτομο δίνει ένα ηλεκτρόνιο σε ένα άλλο άτομο. Τα άτομα που συνδέονται μεταξύ τους με αυτόν τον τρόπο ονομάζονται ιωνικός ενώσεις.
Απλώς, πώς περιγράφεις έναν ομοιοπολικό δεσμό;
ΕΝΑ ομοιοπολικό δεσμό , που ονομάζεται επίσης μοριακός δεσμός , είναι χημικό δεσμός που περιλαμβάνει την κοινή χρήση ζευγών ηλεκτρονίων μεταξύ των ατόμων. Αυτά τα ζεύγη ηλεκτρονίων είναι γνωστά ως κοινόχρηστα ζεύγη ή συγκόλληση ζεύγη, και η σταθερή ισορροπία ελκτικών και απωστικών δυνάμεων μεταξύ των ατόμων, όταν μοιράζονται ηλεκτρόνια, είναι γνωστή ως ομοιοπολικός δεσμός.
Τι είναι ο ομοιοπολικός δεσμός και δώστε παραδείγματα;
Παραδείγματα ενώσεων που περιέχουν μόνο ομοιοπολικούς δεσμούς είναι μεθάνιο (CH4), μονοξείδιο του άνθρακα (CO) και μονοβρωμιούχο ιώδιο (IBr). Ομοιοπολικός δεσμός μεταξύ ατόμων υδρογόνου: Δεδομένου ότι κάθε άτομο υδρογόνου έχει ένα ηλεκτρόνιο, μπορούν να γεμίσουν τα εξωτερικά κελύφη τους μοιράζοντας ένα ζεύγος ηλεκτρονίων μέσω ενός ομοιοπολικό δεσμό.
Συνιστάται:
Πώς διαφέρει ένας ομοιοπολικός δεσμός από ένα κουίζ ιοντικού δεσμού;

Η διαφορά μεταξύ ενός ιοντικού και ενός ομοιοπολικού δεσμού είναι ότι ένας ομοιοπολικός δεσμός σχηματίζεται όταν δύο άτομα μοιράζονται ηλεκτρόνια. Οι ιοντικοί δεσμοί είναι δυνάμεις που συγκρατούν τις ηλεκτροστατικές δυνάμεις έλξης μεταξύ αντίθετα φορτισμένων ιόντων. Οι ιοντικοί δεσμοί έχουν διαφορά ηλεκτραρνητικότητας μεγαλύτερη ή ίση με 2
Τι σημαίνει ομοιοπολικός δεσμός;

Ένας ομοιοπολικός δεσμός, που ονομάζεται επίσης μοριακός δεσμός, είναι ένας χημικός δεσμός που περιλαμβάνει την κοινή χρήση ζευγών ηλεκτρονίων μεταξύ των ατόμων. Για πολλά μόρια, η κοινή χρήση ηλεκτρονίων επιτρέπει σε κάθε άτομο να αποκτήσει το ισοδύναμο ενός πλήρους εξωτερικού κελύφους, που αντιστοιχεί σε μια σταθερή ηλεκτρονική διαμόρφωση
Πώς βρίσκετε κλίση για ανδρείκελα;
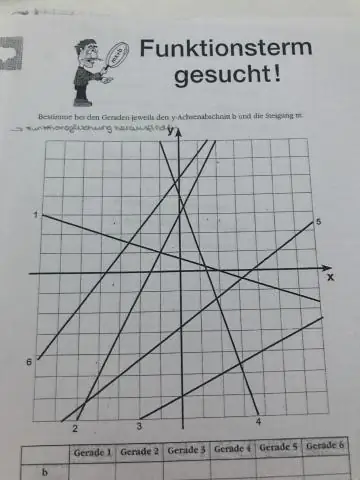
Πράγματα που πρέπει να θυμάστε Κλίση = αλλαγή στο y έναντι της αλλαγής στο x. Κλίση = (y2 - y1)/(x2 - x1) Κλίση = άνοδος κατά τη διαδρομή. Μπορείτε να επιλέξετε οποιαδήποτε δύο σημεία σε μια γραμμή για να υπολογίσετε την κλίση. Μπορείτε να ελέγξετε ξανά την απάντησή σας δοκιμάζοντας διαφορετικά σημεία στη γραμμή. Εάν η γραμμή ανεβαίνει, από αριστερά προς τα δεξιά, η κλίση είναι θετική
Το μεθάνιο είναι πολικός ή μη πολικός ομοιοπολικός δεσμός;

Το μεθάνιο (CH4) είναι μια μη πολική ένωση υδρογονάνθρακα που αποτελείται από ένα μόνο άτομο άνθρακα και 4 άτομα υδρογόνου. Το μεθάνιο είναι μη πολικό καθώς η διαφορά στις ηλεκτραρνητικότητα μεταξύ άνθρακα και υδρογόνου δεν είναι αρκετά μεγάλη για να σχηματίσει έναν πολωμένο χημικό δεσμό
Ποιος ομοιοπολικός δεσμός αποτελείται από 2 κοινά ηλεκτρόνια;

Οι ομοιοπολικοί δεσμοί μπορεί να είναι απλοί, διπλοί και τριπλοί δεσμοί. Οι απλοί δεσμοί εμφανίζονται όταν δύο ηλεκτρόνια μοιράζονται και αποτελούνται από έναν δεσμό σίγμα μεταξύ των δύο ατόμων. Διπλοί δεσμοί εμφανίζονται όταν τέσσερα ηλεκτρόνια μοιράζονται μεταξύ των δύο ατόμων και αποτελούνται από έναν δεσμό σίγμα και έναν δεσμό pi
