
- Συγγραφέας Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Τελευταία τροποποίηση 2025-01-22 16:57.
Ο νόμος για το ιδανικό αέριο, όπως λέει και η παροιμία, είναι στην πραγματικότητα Φ/Β = nRT , με όλες τις τυπικές μεταβλητές. Εδώ n=m/M, όπου m είναι η μάζα του αερίου και M είναι το μοριακό βάρος του αερίου. Με λίγα λόγια το R in Φ/Β = nRT μειώνεται από τον παράγοντα M (μοριακό βάρος) για να εισέλθει το R Φ/Β = mRT.
Απλώς, τι είναι ίσο με το r στο pV nRT;
Ο νόμος του ιδανικού αερίου είναι: pV = nRT , όπου n είναι ο αριθμός των κρεατοελιών, και R είναι καθολική σταθερά αερίου. Η αξία του R εξαρτάται από τις εμπλεκόμενες μονάδες, αλλά συνήθως αναφέρεται με μονάδες S. I. ως: R = 8,314 J/mol. Αυτό σημαίνει ότι για τον αέρα, μπορείτε να χρησιμοποιήσετε την τιμή R = 287 J/kg.
Ομοίως, τι σημαίνει το R στη χημεία pV nRT; Οι μονάδες της καθολικής σταθεράς αερίου R προέρχεται από την εξίσωση PV=n R Τ. Το περίπτερα για την Regnault.
Από αυτή την άποψη, τι σημαίνει το N στο pV nRT;
. Ένας φυσικός νόμος που περιγράφει τη σχέση των μετρήσιμων ιδιοτήτων ενός ιδανικού αερίου, όπου P (πίεση)× V (όγκος) = (αριθμός γραμμομορίων) × R (η σταθερά αερίου) × T (θερμοκρασία σε Kelvin). Προέρχεται από το συνδυασμό των νόμων αερίων του Boyle, του Charles και του Avogadro. Ονομάζεται επίσης καθολικός νόμος αερίων.
Τι είναι το M στον νόμο του ιδανικού αερίου;
Το πρωτότυπο νόμος για το ιδανικό αέριο χρησιμοποιεί τον τύπο PV =nRT, την έκδοση πυκνότητας του νόμος για το ιδανικό αέριο είναι PM = dRT, όπου P είναι η πίεση που μετριέται σε ατμόσφαιρες (atm), T είναι η θερμοκρασία μετρούμενη σε Kelvin (K), R είναι η νόμος για το ιδανικό αέριο σταθερά0,0821 σε Μ (ΜΕΓΑΛΟ) Μ ol(K) ακριβώς όπως στον αρχικό τύπο, αλλά Μ είναι τώρα η μοριακή μάζα (g Μ ol
Συνιστάται:
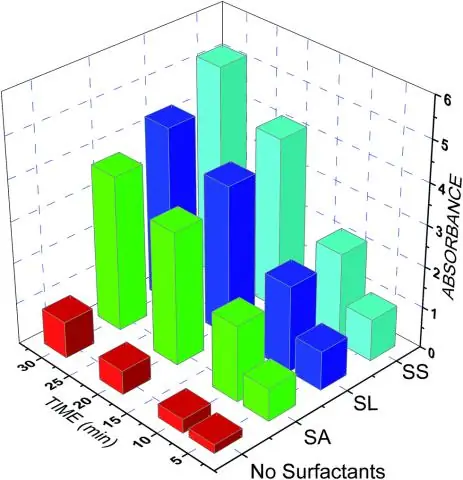
Ποια είναι η διαφορά και η ομοιότητα μεταξύ χρωματογραφίας στήλης και TLC;
Η κύρια «διαφορά» μεταξύ αυτών των δύο είναι ότι ως «χρωματογραφία λεπτής στιβάδας» χρησιμοποιείται διαφορετική στατική φάση από τη χρωματογραφία στήλης. Μια άλλη διαφορά είναι ότι η «χρωματογραφία λεπτής στιβάδας» μπορεί να χρησιμοποιηθεί για τη διάκριση μη πτητικών μιγμάτων, κάτι που δεν είναι δυνατό στη χρωματογραφία στήλης»
Ποια είναι η διαφορά μεταξύ άλφα και βήτα και γάμμα;

Τα σωματίδια άλφα είναι ενεργητικοί (γρήγοροι) πυρήνες ηλίου, τα σωματίδια βήτα είναι μικρότερα και έχουν το μισό φορτίο, όντας ενεργητικά ηλεκτρόνια (ή ποζιτρόνια) μόνο τα σωματίδια γάμμα είναι φωτόνια, δηλαδή, δεν είναι καθόλου σωματίδια με μάζα, είναι μια μορφή ηλεκτρομαγνητικού ακτινοβολία, μια μορφή πιο ενεργητική από τις ακτίνες Χ
Ποια είναι η διαφορά μεταξύ του ορισμού του Arrhenius και του ορισμού του brønsted Lowry για τα οξέα και τις βάσεις;

Η διαφορά μεταξύ των τριών θεωριών είναι ότι η θεωρία Arrhenius δηλώνει ότι τα οξέα περιέχουν πάντα Η+ και ότι οι βάσεις περιέχουν πάντα ΟΗ-. Ενώ το μοντέλο Bronsted-Lowry ισχυρίζεται ότι τα οξέα είναι δότες πρωτονίων και δέκτες pron, επομένως οι βάσεις δεν χρειάζεται να περιέχουν OH- έτσι τα οξέα δίνουν ένα πρωτόνιο στο νερό που σχηματίζει H3O+
Τι είναι ένας δομικός τύπος Ποια είναι η διαφορά μεταξύ ενός δομικού τύπου και ενός μοριακού μοντέλου;
Ένας μοριακός τύπος χρησιμοποιεί χημικά σύμβολα και δείκτες για να υποδείξει τον ακριβή αριθμό των διαφορετικών ατόμων σε ένα μόριο ή ένωση. Ένας εμπειρικός τύπος δίνει την απλούστερη, ακέραια αναλογία ατόμων σε μια ένωση. Ένας δομικός τύπος υποδεικνύει τη διάταξη σύνδεσης των ατόμων στο μόριο
Ποια είναι η διαφορά μεταξύ της μικροεξέλιξης και της μακροεξέλιξης Ποια είναι μερικά παραδείγματα από το καθένα;

Μικροεξέλιξη εναντίον Μακροεξέλιξης. Παραδείγματα τέτοιων μικροεξελικτικών αλλαγών θα περιλαμβάνουν μια αλλαγή στο χρώμα ή το μέγεθος ενός είδους. Η μακροεξέλιξη, αντίθετα, χρησιμοποιείται για να αναφέρεται σε αλλαγές σε οργανισμούς που είναι αρκετά σημαντικές ώστε, με την πάροδο του χρόνου, οι νεότεροι οργανισμοί να θεωρούνται εντελώς νέο είδος
